Axit là gì?
Axit là một chất hóa học có cấu trúc phân tử chứa một hoặc nhiều nguyên tử hydro gắn với nhóm axit (như -Cl, =SO₄, -NO₃). Các nguyên tử hydro này có thể thay thế bởi nguyên tử kim loại, tạo ra muối.

Đọc thêm: Áp suất là gì? Công thức tính, phân loại và ý nghĩa trong thực tiễn
Đặc điểm tính chất hóa lý của axit
Tính chất hóa học của axit
Thay đổi màu của chất chỉ thị: Axit có khả năng làm thay đổi màu sắc của một số chất chỉ thị như quỳ tím, giấy thử pH và dung dịch phenolphtalein.
Phản ứng với kim loại: Một số axit có thể phản ứng với kim loại, tạo thành muối và giải phóng khí hydro. Ví dụ, axit sulfuric (H₂SO₄) và axit nitric (HNO₃) đặc, khi nóng, có thể tác dụng với hầu hết các kim loại, sinh ra lưu huỳnh dioxit (SO₂) hoặc nitơ dioxit (NO₂):
HCl + Fe → FeCl₂ + H₂
2Fe + 6H₂SO₄ → Fe₂(SO₄)₃ + 6H₂O + 3SO₂
Phản ứng với bazơ: Axit phản ứng với bazơ để tạo ra muối và nước theo phương trình:
Cu(OH)₂ + H₂SO₄ → CuSO₄ + 2H₂O
Phản ứng với oxit bazơ: Axit có thể phản ứng với oxit bazơ để tạo ra muối và nước:
Na₂O + 2HCl → 2NaCl + H₂O
FeO + H₂SO₄ (loãng) → FeSO₄ + H₂O
CuO + 2HCl → CuCl₂ + H₂O
Phản ứng với muối: Axit cũng có thể tác dụng với một số muối, tạo ra muối mới và axit mới.
Tính chất vật lý của axit
Hầu hết các axit đều dễ dàng hòa tan trong nước, tạo ra dung dịch có vị chua đặc trưng. Chính vì vậy, các loại trái cây chứa axit tự nhiên như cam, chanh, hay dứa thường mang vị chua.
Khi tiếp xúc với axit mạnh, đặc biệt là các axit đậm đặc, có thể gây cảm giác đau rát hoặc bỏng do tính ăn mòn của axit đối với da và niêm mạc. Vì vậy, khi làm việc với axit, cần đeo các thiết bị bảo vệ như găng tay và kính bảo hộ.
Axit là một loại chất điện ly, nghĩa là khi hòa tan trong nước, chúng sẽ phân ly thành các ion, giúp dung dịch có khả năng dẫn điện. Tính chất này được ứng dụng trong nhiều lĩnh vực, đặc biệt trong công nghệ pin và điện phân.
Đọc thêm: Hóa chất là gì? Vai trò, ứng dụng và lưu ý khi sử dụng
Các dạng phân loại của axit
Dựa trên tính chất hóa học của axit
-
Axit mạnh: Bao gồm các axit như axit sulfuric (H₂SO₄), axit clohydric (HCl), axit nitric (HNO₃),... Các axit này khi hòa tan trong nước sẽ phân ly hoàn toàn, tạo ra dung dịch có tính axit rất mạnh với độ pH thấp hơn nhiều so với 7. Chúng có khả năng ăn mòn mạnh mẽ và thường được ứng dụng trong các ngành công nghiệp hóa chất, luyện kim và sản xuất phân bón.
-
Axit yếu: Ví dụ như axit cacbonic (H₂CO₃) và hydro sulfua (H₂S). Khi hòa tan trong nước, chúng chỉ phân ly một phần, tạo ra dung dịch có pH gần bằng 7. Vì tính axit yếu, chúng ít gây ăn mòn hơn và thường xuất hiện trong tự nhiên, như trong nước có ga hoặc khí thải từ quá trình phân hủy hữu cơ.
Dựa trên thành phần oxy
-
Axit không chứa oxy: Đây là nhóm axit có phân tử chỉ bao gồm nguyên tử hydro gắn trực tiếp với một nguyên tố khác mà không có oxy. Ví dụ tiêu biểu của nhóm này là axit clohydric (HCl), axit hiđroiodic (HI), axit hiđrosunfua (H₂S), axit hiđrobromic (HBr) và axit flohiđric (HF).
-
Axit chứa oxy: Đây là nhóm axit có nguyên tử oxy trong phân tử, thường liên kết với nguyên tố trung tâm. Một số axit điển hình thuộc nhóm này là axit sulfuric (H₂SO₄), axit photphoric (H₃PO₄), axit cacbonic (H₂CO₃) và axit nitric (HNO₃). Các axit này đóng vai trò quan trọng trong nhiều lĩnh vực như công nghiệp, nông nghiệp và sinh học.
Phân loại axit theo nguồn gốc
-
Axit vô cơ: Là nhóm axit có nguồn gốc từ khoáng chất, không chứa liên kết cacbon-hydro đặc trưng của hợp chất hữu cơ. Một số axit vô cơ phổ biến bao gồm axit clohydric (HCl), axit nitric (HNO₃) và axit sulfuric (H₂SO₄). Chúng có tính ăn mòn cao và được sử dụng rộng rãi trong công nghiệp, thí nghiệm hóa học và sản xuất phân bón.
-
Axit hữu cơ: Là nhóm axit có chứa nhóm -COOH (cacboxyl) trong cấu trúc phân tử, thường xuất hiện trong các sinh vật sống. Một số ví dụ tiêu biểu là axit fomic (HCOOH) và axit axetic (CH₃COOH), vốn có mặt trong giấm ăn và nhiều quá trình sinh học. So với axit vô cơ, axit hữu cơ thường có tính axit yếu hơn và ít ăn mòn hơn.

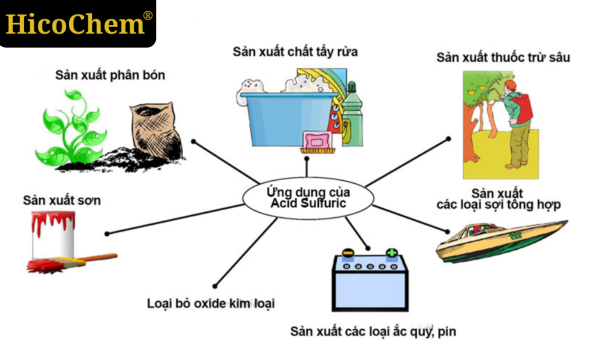
Ứng dụng của axit trong các lĩnh vực khác nhau
Axit có vai trò quan trọng trong nhiều lĩnh vực, từ công nghiệp, y học đến thực phẩm và sinh học. Sau đây là một số ứng dụng tiêu biểu của axit:
Ứng dụng trong công nghiệp
Axit thường được dùng để làm sạch bề mặt kim loại, loại bỏ gỉ sét và hạn chế quá trình ăn mòn.
Axit sulfuric (H₂SO₄) là thành phần thiết yếu trong chất điện phân, được dùng trong sản xuất pin cho xe ô tô.
Axit cacboxylic có thể phản ứng với rượu tạo thành este, hợp chất có mùi thơm, được ứng dụng phổ biến trong ngành công nghiệp mỹ phẩm và thực phẩm.
Các axit mạnh như H₂SO₄, HCl, HNO₃ có vai trò quan trọng trong ngành hóa chất và chế biến khoáng sản.
Axit clohydric (HCl) được ứng dụng trong ngành dầu mỏ, hỗ trợ quá trình khoan giếng dầu và tăng cường hiệu suất khai thác.
Trong lĩnh vực kim hoàn, hỗn hợp HCl và HNO₃ đậm đặc (tỷ lệ 3:1) gọi là nước cường toan, có khả năng hòa tan vàng và bạch kim, hỗ trợ quá trình tinh chế kim loại quý.
Ứng dụng trong thực phẩm
Axit là một chất phụ gia quan trọng trong ngành chế biến và bảo quản thực phẩm, đặc biệt trong các loại nước giải khát có ga và thực phẩm đóng hộp, giúp kiểm soát độ pH và kéo dài thời gian bảo quản.
Ứng dụng trong nông nghiệp
Axit còn được sử dụng trong sản xuất phân bón, ví dụ như amoni nitrat (NH₄NO₃), được sản xuất từ phản ứng giữa amoniac (NH₃) và axit nitric (HNO₃).
Ứng dụng trong y học
Axit acetylsalicylic (aspirin) được dùng làm thuốc giảm đau, hạ sốt và chống viêm.
Axit boric có tính khử trùng, giúp điều trị vết thương nhỏ, bỏng nhẹ, và cũng có thể pha loãng để làm dung dịch rửa mắt. Axit boric còn được sử dụng trong điều trị mụn trứng cá, bệnh phồng rộp chân của vận động viên, và bảo quản mẫu nước tiểu trong phòng thí nghiệm.
Ứng dụng trong sinh học
Axit amin là thành phần quan trọng trong quá trình tổng hợp protein, hỗ trợ sửa chữa mô và phát triển cơ thể ở các sinh vật.
Axit nucleic (ADN và ARN) có vai trò then chốt trong việc lưu trữ và truyền đạt thông tin di truyền, đảm bảo sự di truyền đặc điểm qua các thế hệ.
Axit cacbonic (H₂CO₃) giúp duy trì sự cân bằng pH trong cơ thể, đảm bảo hoạt động ổn định của các hệ thống sinh hóa bên trong.








TVQuản trị viênQTV
Chào mừng, quý khách. Hãy để lại nhận xét, chúng tôi sẽ trả lời sớm